|
酸性、中性、アルカリ性で色素の色が変化することが、これまでのQ&Aにたくさん出てきました。赤キャベツの汁、紅茶にレモンを入れたとき、などです。純粋な水は中性ですが、酸を入れると酸性になります。でも、どの程度酸性なのかを表すのが難しいので、pH(ピーエッチ、昔はペーハーと言ってました。pは小文字で、PHはピンチヒッターになってしまう。)の値で表すのです。正確に水のpHを求めるにはpH測定器を用いますが、リトマス紙のようなpH試験紙を用いると色の変化から簡単におおよそのpHを知ることができます。pHについては堀場製作所のホームページにやさしく詳しい説明がありますので、そこからお許しを得て引用させて頂きます。
(http://global.horiba.com/story/ph/index.htm)
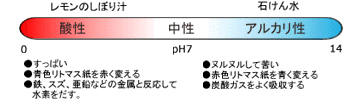
まず、酸性、中性、アルカリ性ですが、水は中性で、レモンのしぼり汁(クエン酸)を入れると酸性になります。また、石けん水を入れると弱いですがアルカリ性になり、カセイソーダを入れると強いアルカリ性になります。
|
|
|
酸性、中性、アルカリ性
|
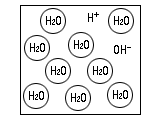
水はH2Oで表される分子ですが、じつは一部H+とOH-のイオンに分かれていて、H2Oになったりイオン(+や-の電荷を持ったもの)になったりしているのです(平衡と言います)。pHとは水素イオン(H+)の濃度のことなんです。濃度とは水1リットル中にある水素イオンの量です。
水はH+とOH-に分かれている
|
|
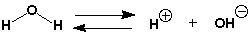 |
温度が一定であると、中性の水では水素イオン濃度[H+]と水酸イオン濃度[OH-]の間には次の関係があります([
]は濃度を示し、Kwは水の解離定数とよばれます)。
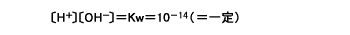
H+もOH-もH2Oから分かれたものですから、濃度は同じですので、次のようになります。
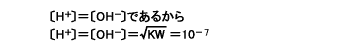
ですから、中性の水の水素イオン濃度は、10-7 mol/lですが、指数ですのでこれではややこしくなります。そこで、水素イオン濃度の対数をとって、マイナスをつけたものをpHとするのです。すると、中性の水のpHはよく見慣れた数字の7になり、酸性では7より小さな値、アルカリ性では7より大きな値になります。
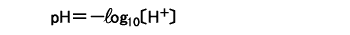 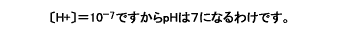
pHは水素イオン濃度を対数で表しているので、pHと水素イオン濃度の間には大きな違いがあります。例えば、pH4の水溶液には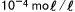 (1リットル中に0.0001モル)の水素イオンが含まれますが、pH6では (1リットル中に0.0001モル)の水素イオンが含まれますが、pH6では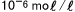 (1リットル中に0.000001モル)の水素イオンが含まれているのです。pHは2しか違いませんが、水素イオン濃度は100倍違うのです。 (1リットル中に0.000001モル)の水素イオンが含まれているのです。pHは2しか違いませんが、水素イオン濃度は100倍違うのです。
pHはガラス電極を用いた「pHメーター」を用いて測定するのですが、その原理はどうなっているのでしょうか。ガラス電極法とは、ガラス電極と比較電極の2本の電極を用い、この2つの電極の間に生じた電圧(電位差)を知ることで、ある溶液のpHを測定する方法です。
ガラスの薄膜の内・外側にpHの異なる溶液があると、薄膜部分に、pHの差に比例した起電力が生じます。この薄膜を電極膜といいます。
普通、溶液が30℃の場合、2つの溶液のpHの差が1違えば、約60mVの 起電力が生じます。通常、ガラス電極の内部液にはpH7の液を用いますので、電極膜に生じた起電力を測定すれば、被検液、つまりpHを求めたい溶液のpH値がわかるわけです。
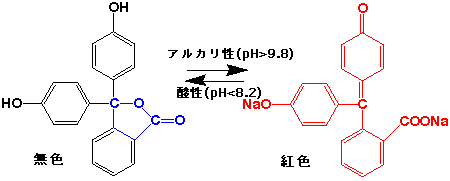
pHは色素の指示薬を用いても知ることができます。フェノールフタレインは酸性、中性(pH < 8.2)で無色で、アルカリ性(pH
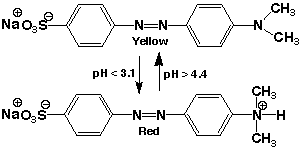
> 9.8)で赤色になります。メチルオレンジは酸性指示薬で、強い酸性(pH < 3.1)で赤色、中性、アルカリ性(pH >
4.4)で黄色となります。(指示薬の詳細はQ 43を見てください)
|
|
|
フェノールフタレイン(アルカリ性指示薬)
|
| |
|
|
|
メチルオレンジ(酸性指示薬)
|
古くから知られるリトマス試験紙はある種の地衣類から取った紫色の色素(アゾリトミン azolitmin)を紙にしみ込ませたもので、pH
< 4.5で赤、pH > 8.3で青になります。青色リトマス紙は色素をアンモニアで青変させてからろ紙に浸し乾燥させたもので、酸性溶液で赤くなります。また、赤色リトマス紙は塩酸で赤変させた色素をろ紙に浸し乾燥させたもので、アルカリ溶液で青色になります。
|