|
色素には水に溶ける染料と、水に溶けない顔料とがあります。また、水には溶けないが油には溶けるものもあります。
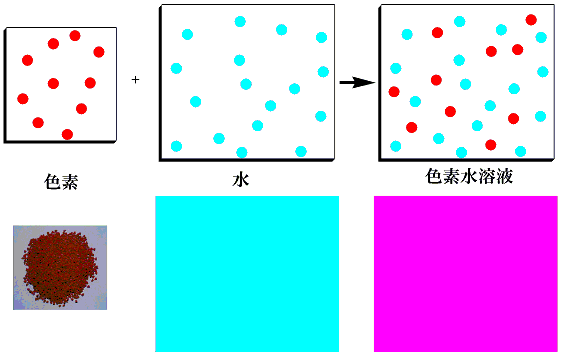
水に溶ける水溶性色素は、水に加えると、最初はもやもやとして均一ではありませんが、時間が経つと液全体に全体に広がって色のついた液体になります。たとえば、ベニコウジ色素を水に溶かすと、きれいな溶液になります。
|

|

|
|
ベニコウジ色素(モナスカス色素)Monascus colour
|
ベニコウジ色素溶液
|
キリヤ化学では食用色素を販売していますが、水によく溶ける食用色素と水にあまり溶けずに油に溶けやすい色素があります。
例えば、「マリーゴールド色素」の製法は、「キク科マリーゴールドの花より、室温時ヘキサンで抽出して得られたものである。」と書いてありますが、油であるヘキサンを用いて抽出しているので、油に溶ける色素であることが分かります。
赤キャベツの色素である「赤キャベツ色素」は、「アブラナ科キャベツの赤い葉(赤キャベツ、紫キャベツ)より、室温時弱酸性水溶液で抽出して得られたものである。」と書いてあります。ここで、「弱酸性水溶液」とは、たとえば薄い塩酸などを少し加えた水のことです。したがって、アントシアニン系色素である赤キャベツ色素は水に溶ける水溶性色素です。
同じページに、アカキャベツ色素溶液の写真がありますが、その説明に、キリヤスレッドRC-Y、クエン酸緩衝液(pH3)(添加量0.08%)
とあります。クエン酸とは、レモンなどに含まれる酸っぱい成分です。食用色素ですので、塩酸ではなく、クエン酸を加えて酸性の水にしているのです。
アカキャベツ色素の重さを、0.08%になるように量り、水に加えればいいのですが、あまりにも微量ですので、あらかじめ濃い溶液を作り、これを0.08%になるように薄めて溶液を作っています。
|
|
|
色素水溶液の調整
|
このような色のついた液体を、元の色素と透明な水に戻せるかが質問だと思います。さて、このような溶液から、元の色素と水に戻せるでしょうか?これは非常に難しい問題です。
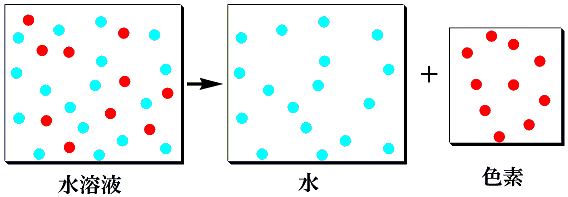
まず、どうして色素が全体に広がって、着色した液体になるのかを考えてみます。
この現象を理解するには、物理と化学の合わさった「物理化学」を勉強する必要があります。
色素を水に溶かすと、色素分子と水分子が衝突して、色素はあちこちに動いてしまいます。これを拡散と言います。色素は粉末ですが、その最小単位は分子です。
(1)先ず、色素の1分子を真空の容器に入れてみます。分子は結晶状態、絶対零度でない限り、運動をしていますので、色素分子は容器の中を動き回ります。
(2)ここに水の分子を入れてやると、色素と水の分子がそれぞれ動き回り、ぶつかったりします。
(3)水や色素が多いと、上のような色素溶液ができます。色素分子は水分子に衝突しながら動き回っていますので、全体として均一な状態になっています。これが、色素分子が水の中で拡散した状態です。
ここで、物理化学の法則がでてきます。「エントロピー増大則」という「熱力学第2法則」です。エントロピーとは無秩序を表す度合いです。色素分子は水分子の中ででたらめに動き回り、無秩序の状態になっています。
魚を飼う水槽に、コーヒーを加えると、「エントロピー増大則」にしたがってコーヒーは水槽全体に広がり、何日経っても元には戻りません。
熱いお湯を冷たい水に加えると、熱い水分子は、冷たい水分子と衝突して広がった状態になります。従って、熱は広がって、全体としてお湯は冷たくなります。
学校の校庭に、昼休みになって生徒が出て行くと、クラスごとではなくみんながばらばらに広がります。授業中の教室では先生が見ているので、秩序があって生徒は席に座っていたものが、昼休みになると秩序が無くなり、ばらばらになります。元の秩序がある席にみんなが座るには、先生の声、鐘の音などのエネルギーを加えてやる必要があるのです。席に座っているときは動き回れませんので、自由度は小さくエントロピーは小さいのです。ところが、休み時間になると、自由度が大きくエントロピーが大きくなり自由に動き回れるようになります。世の中の現象では自由度が大きくエントロピーが大きいように変化していくのです。
色素を水に混ぜると、でたらめに拡散して無秩序になり、元には戻らないことを示しています。色素の溶液から色素だけを取り出すことは、熱力学第2法則で無理だと言うことが分かったと思います。
それでも、色素と水を分離することはできないのでしょうか?いくつかの方法があります。その答えは次のQ&Aで。
|