|
染料には多くの種類があり、化学構造や染色方法により分類されていますが、アゾ染料を化学構造から簡単に分類すると、酸性染料と塩基性染料になります。
 |
|
 |
|
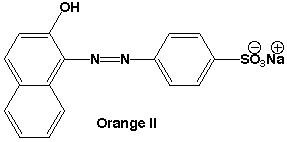
酸性染料
|
|
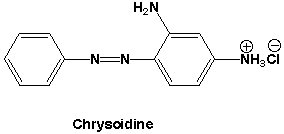
塩基性染料
|
酸性染料にはスルホン酸(-SO3H)やカルボン酸(-COOH)が含まれていますので、中性の水溶液中ではマイナスの荷電を持っています。一方、塩基性染料にはアミノ基(-NH2)が含まれているので、中性の水溶液中ではプラスの荷電を持っています。さて、このような染料が酸性やアルカリ性で溶けたり溶けなかったりするのはなぜでしょう?
|
|
|
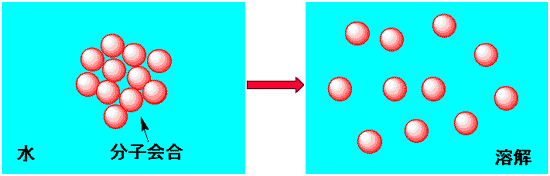
染料分子が集まると溶けない
|
分子がバラバラになると溶ける
|
まず、水に溶けるとはどういうことかを考えてみます。染料分子が集まった状態は溶けていない状態です。染料分子がひとつずつバラバラになった状態が溶けた状態です。液が濁っているとか透明であるとかは関係ありません。染料分子の固まりの大きさが光の波長よりも小さいと透明ですが、溶けているわけではありません。
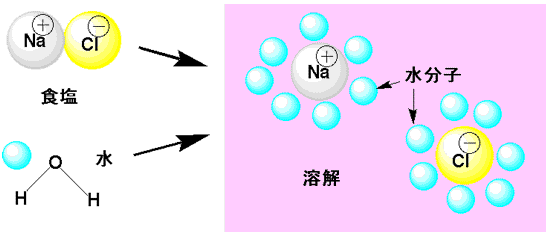
水によく溶ける食塩で考えてみます。固体の食塩では、ナトリウム(Na)のプラスと塩素(Cl)のマイナスが引き合ってくっついています。これを水に加えると、ナトリウムの周りに水の分子がくっついて取り囲みます。塩素の周りにも水の分子が取り囲みます。これで、ナトリウムと塩素は引き離されてバラバラになり、溶けたことになります。水はプラスでもマイナスでもありませんが、部分的に水素(H)がプラスに、酸素(O)がマイナスになっていると考えられますので、プラスやマイナスのイオンとくっつくのです。
 |
|
固体の食塩
|
食塩が水に溶けた状態
|
次に、酸性染料は酸性やアルカリ性でどうなるのかを考えてみます。酸性染料に付いているのはスルホン酸ナトリウムで、スルホン基はマイナスに、ナトリウムはプラスになっています。これは丁度食塩と同じ状態です。ですから、水に加えると水分子がそれぞれ付いて、染料分子はバラバラになり溶けます。
酸性染料の溶解と酸性アルカリ性の変化
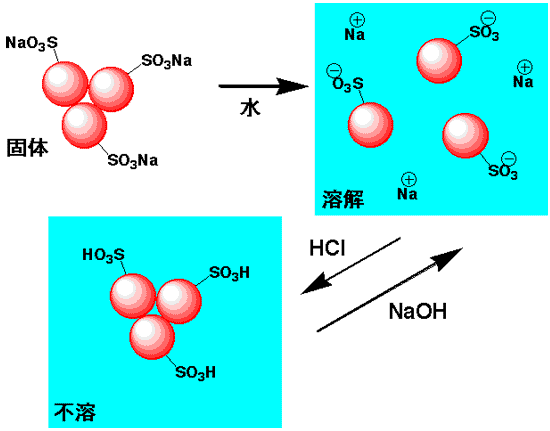 |
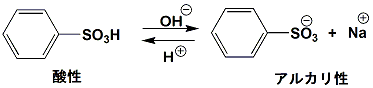
染料が溶けたアルカリ性の溶液に塩酸を加えて酸性にしてみます。塩酸のCl-がNa+とくっつき、塩酸のH+が-SO3-に付いて、-SO3Hになります。-SO3Hはイオンにはなっていませんので水が付くことができず、染料分子は集まった状態になり、染料は溶けません。もしこの溶液に布を漬けておくと、染料は布に着き、染色されることになるのです。
酸性染料の酸性、アルカリ性での変化
 |
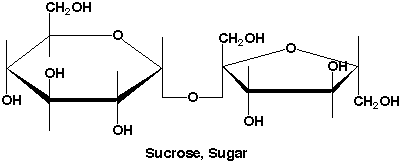
砂糖も水によく溶けますが、イオンになっているのでしょうか?砂糖はイオンにはなっていません。砂糖の分子には水酸基(-OH)があるので、水によく溶けるのです。水によく溶けるアルコールにも水酸基があります。水の分子は、H-OHですから、水酸基と似ていますね。ですから、水は水酸基にくっつくことができ、砂糖の分子をバラバラにして水に溶かすことができるのです。
砂糖
|
|
ところで、塩基性染料は酸性でプラスに荷電してイオンになり、アルカリ性ではイオンにはなりません。したがって、酸性では水によく溶け、アルカリ性では水に溶けません。酸性染料とは逆の関係です。
塩基性染料の酸性、アルカリ性での変化
|
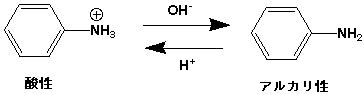
|
|